LES ÉTATS EXCEPTIONNELS DE LA MATIÈRE
Publié le 28/10/2011

Extrait du document
Les conditions de température et de pression qui règnent sur notre planète sont exceptionnelles et permettent à la vie de s'y maintenir et même de s'y développer. Si la température était trop élevée, les liquides organiques qui constituent la majeure partie des tissus vivants entreraient en ébullition et il en serait de même à très basse pression.
«
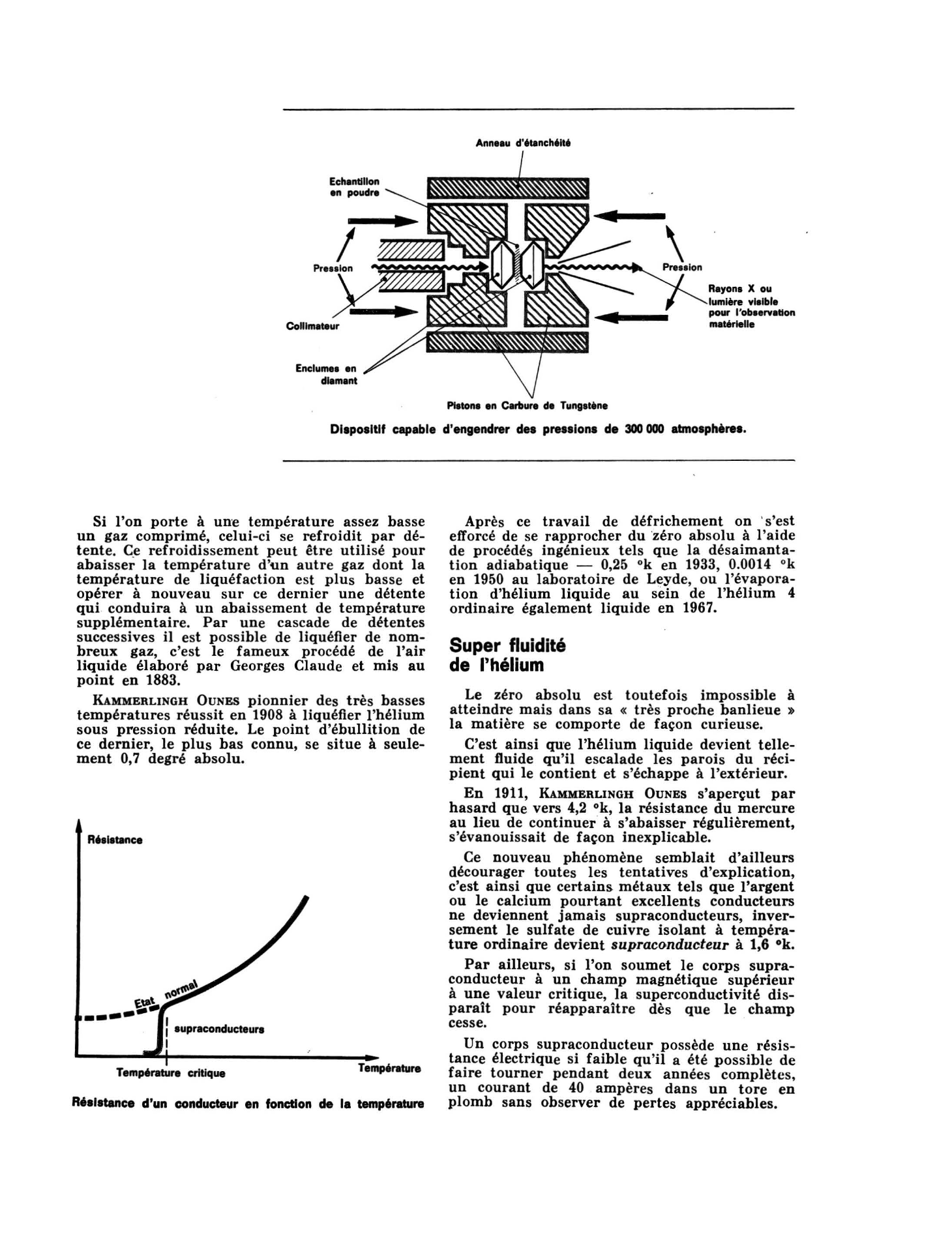
Echllntillon en poudre
•
DlapoaiUf capable d'engendrer dea preaalona de 300 000 atmoeph•rea.
Si l'on porte à une température assez basse un gaz comprimé, celui-ci se refroidit par dé tente .
C_e refroidissement peut être utili s é pour abaisser la température d'un autre gaz dont la température de liquéfaction e st plus basse et opérer à nouveau sur ce dernier une détente qui conduira à un abaissement de température supplémentaire.
Par une cascade de détentes successives il e st possible de liquéfier de nom breux gaz, c' est le fameux procédé de l'air liquide élaboré par Georges Claude et mis au point en 1883.
KAMMERLINGH ÛUNES pionnier des très basses températures réussit en 1908 à liquéfier l'hélium sous pression réduite.
Le point d'ébullition de
ce dernier, le plus bas connu, se situe à seule ment 0, 7 degré absolu.
RHiaiMice
Tempjmure critique
R6eletance d'un conducteur en fonction de la temp6rature
Aprè s ce travail de défrichement on 's'est efforcé de se rapprocher du zéro absolu à l'aide de procédés ingénieux tels que la désaimanta tian adiabatique - 0,25 •k en 1933 , 0.0014 •k en 1950 au laboratoire de Leyde, ou l'évapora tion d'hélium liquide au sein de l'hélium 4 ordinaire également liquide en 1967.
Super fluidité
de
l'hélium
Le zéro absolu est toutefois impossible à atteindre mais dans sa « très proche banlieue » la matière se comporte de façon curieuse.
C'est ainsi que l'hélium liquide devient telle ment fluide qu'il escalade les parois du réci pient qui le contient et s'échappe à l'extérieur.
En 1911 , KAMMERLINGH ÛUNES s'aperçut par hasard que vers 4,2 •k, la résistance du mercure au lieu de continuer à s'abaisser régulièrement, s'évanouissait de façon inexplicable.
Ce nouveau phénomène semblait d'ailleurs décourager toutes les tentatives d'explication, c'est ainsi que certains.
métaux tels que l'argent ou le calcium pourtant excellents conducteurs ne deviennent jamais supraconducteurs, inver sement le sulfate de cuivre isolant à tempéra ture ordinaire devient supraconducteur à 1,6 °k.
Par ailleurs, si l'on soumet le corps supra conducteur à un champ magnétique supérieur à une valeur critique, la superconductivité dis paraît pour réapparaître dès que le champ cesse.
Un corps supraconducteur possède une résis tance électrique si faible qu'il a été possible de faire tourner pendant d eux années complètes, un courant de 40 ampères dans un tore en plomb sans observer de pertes appréciables..
»
↓↓↓ APERÇU DU DOCUMENT ↓↓↓
Liens utiles
- Etats de la matière et changements d'états Récapitulatif Synthèse construite par Sylvain sylvain.
- Thermodynamique chimique Etats de la matière o Définitions o Les états de la matière o Premier principe : U, H o Deuxième principe : S o Enthalpie libre et équilibre Cours complété et exemplifié dans UE spé Pharma P.
- CRISTAUX STRUCTURE DES CRISTAUX DÉFINITION La matière se présente normalement sur la Terre en trois états d'agrégation différents : l'état gazeux (gaz), l'état liquide et l'état solide.
- Thermodynamique chimique Etats de la matière o Définitions o Les états de la matière o Premier principe : U, H o Deuxième principe : S o Enthalpie libre et équilibre Cours complété et exemplifié dans UE spé Pharma P.
- matière, états de la - physique.