Corrige activité empreinte digital et spectre
Publié le 28/05/2023
Extrait du document
«
TP18 –
CTM8
– Comportement de groupe
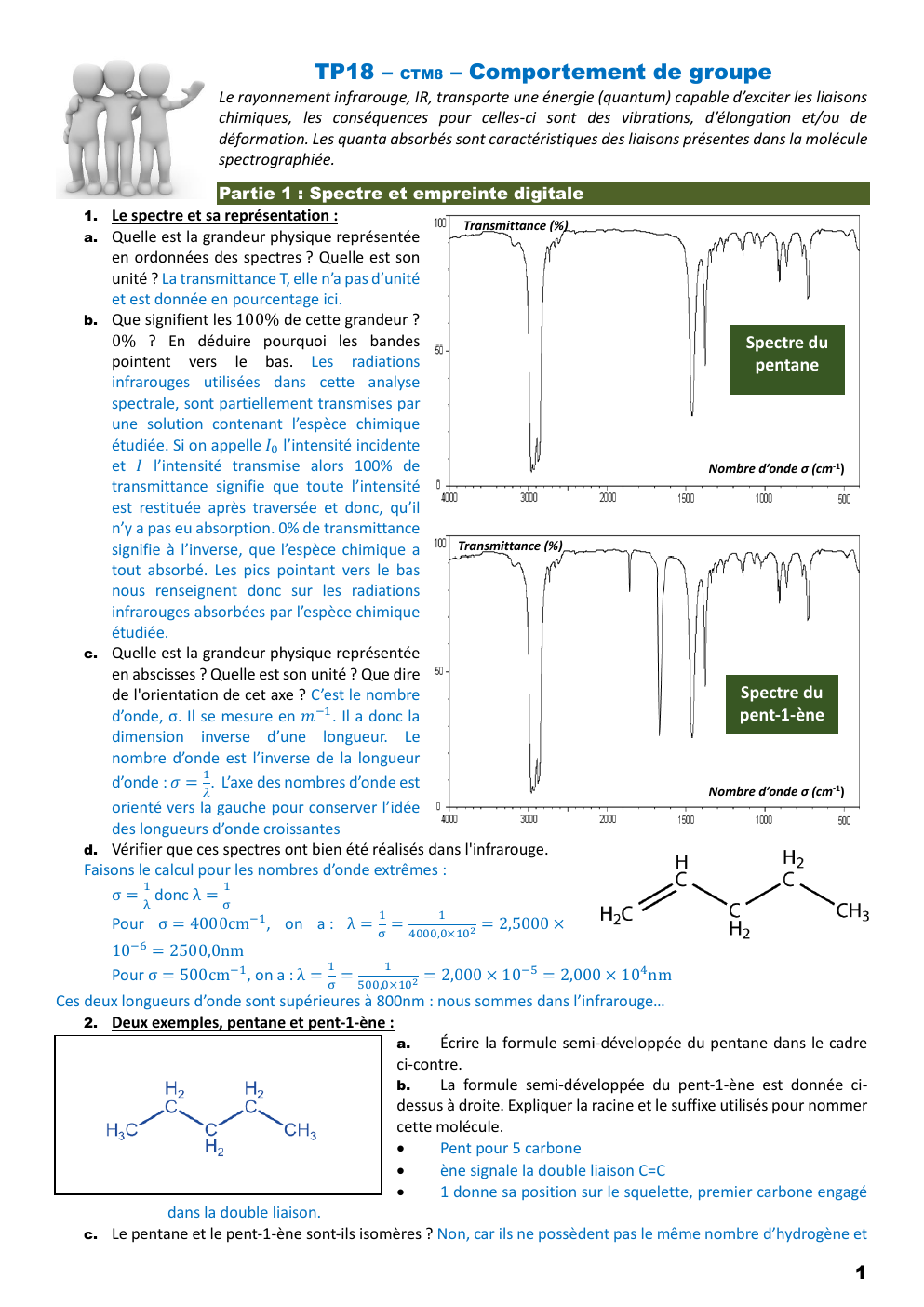
Le rayonnement infrarouge, IR, transporte une énergie (quantum) capable d’exciter les liaisons
chimiques, les conséquences pour celles-ci sont des vibrations, d’élongation et/ou de
déformation.
Les quanta absorbés sont caractéristiques des liaisons présentes dans la molécule
spectrographiée.
Partie 1 : Spectre et empreinte digitale
Le spectre et sa représentation :
Transmittance (%)
Quelle est la grandeur physique représentée
en ordonnées des spectres ? Quelle est son
unité ? La transmittance T, elle n’a pas d’unité
et est donnée en pourcentage ici.
b.
Que signifient les 100% de cette grandeur ?
0% ? En déduire pourquoi les bandes
pointent vers le bas.
Les radiations
infrarouges utilisées dans cette analyse
spectrale, sont partiellement transmises par
une solution contenant l’espèce chimique
étudiée.
Si on appelle 𝐼0 l’intensité incidente
et 𝐼 l’intensité transmise alors 100% de
transmittance signifie que toute l’intensité
est restituée après traversée et donc, qu’il
n’y a pas eu absorption.
0% de transmittance
Transmittance (%)
signifie à l’inverse, que l’espèce chimique a
tout absorbé.
Les pics pointant vers le bas
nous renseignent donc sur les radiations
infrarouges absorbées par l’espèce chimique
étudiée.
c.
Quelle est la grandeur physique représentée
en abscisses ? Quelle est son unité ? Que dire
de l'orientation de cet axe ? C’est le nombre
d’onde, σ.
Il se mesure en 𝑚−1.
Il a donc la
dimension inverse d’une longueur.
Le
nombre d’onde est l’inverse de la longueur
1
d’onde : 𝜎 = 𝜆.
L’axe des nombres d’onde est
orienté vers la gauche pour conserver l’idée
des longueurs d’onde croissantes
d.
Vérifier que ces spectres ont bien été réalisés dans l'infrarouge.
Faisons le calcul pour les nombres d’onde extrêmes :
1
1
σ = λ donc λ = σ
1.
a.
1
Spectre du
pentane
Nombre d’onde σ (cm-1)
Spectre du
pent-1-ène
Nombre d’onde σ (cm-1)
1
Pour σ = 4000cm−1, on a : λ = σ = 4000,0×102 = 2,5000 ×
10−6 = 2500,0nm
1
1
Pour σ = 500cm−1 , on a : λ = σ = 500,0×102 = 2,000 × 10−5 = 2,000 × 104 nm
Ces deux longueurs d’onde sont supérieures à 800nm : nous sommes dans l’infrarouge…
2.
Deux exemples, pentane et pent-1-ène :
a.
Écrire la formule semi-développée du pentane dans le cadre
ci-contre.
b.
La formule semi-développée du pent-1-ène est donnée cidessus à droite.
Expliquer la racine et le suffixe utilisés pour nommer
cette molécule.
•
Pent pour 5 carbone
•
ène signale la double liaison C=C
•
1 donne sa position sur le squelette, premier carbone engagé
dans la double liaison.
c.
Le pentane et le pent-1-ène sont-ils isomères ? Non, car ils ne possèdent pas le même nombre d’hydrogène et
1
donc n’ont pas la même formule brute.
Qu'ont-ils en commun ? Le squelette contient le même nombre de carbone.
Qu'ont-ils de différent ? La double liaison C=C, chaîne saturée pour l’un et insaturée pour l’autre.
Une molécule
comme le pent-1-ène appartient à la famille des alcènes, hydrocarbures possédant des doubles liaisons C=C.
On dit que le squelette est insaturé alors que celui des alcanes est saturé (toutes les valences des carbone du
squelette sont engagés dans des liaisons simples).
f.
Quelle(s) observation(s) peut-on faire en comparant les deux spectres dans les « petits nombres d'onde » ? En
utilisant les réponses précédentes que peut-on en déduire ? Dans l’intervalle allant de 500𝑐𝑚−1 à 1500𝑐𝑚−1,
les deux spectres sont identiques : cette partie correspond donc aux points communs entre les deux molécules
= le squelette.
g.
Quelle(s) observation(s) peut-on faire en comparant les deux spectres dans les « grands nombres d'onde » ?
En utilisant les réponses précédentes que peut-on en déduire ? Les deux spectres diffèrent dans cette partie.
Il y a présence d’un pic d’intensité moyenne à 1660𝑐𝑚−1 pour le pent-1-ène qui n’est pas présent sur le spectre
du pentane.
Par contre les deux spectres présentent une bande commune de forte intensité entre 2800𝑐𝑚−1
et 3000𝑐𝑚−1.
Cette partie du spectre entre 1500𝑐𝑚−1 et 4000𝑐𝑚−1, correspond donc aux différences de structures entre
les molécules.
Chaque bande correspond à un type de liaison.
Voir tables.
h.
En déduire le nombre d'onde correspondant à la bande caractéristique de la liaison C=C.
Comparer avec la
table.
La liaison C=C n’est présente que sur la molécule de pent-1-ène, c’est donc le pic à 1660𝑐𝑚−1.
Confirmation dans la table.
d.
e.
2
Partie 2 : La classe ! …..
D'un alcool
Nous allons comparer....
»
↓↓↓ APERÇU DU DOCUMENT ↓↓↓
Liens utiles
- Activité enseignement scientifique sur les méthodes de stockage de l'énergie
- Activité 7 c: Les polysaccharides, polymérisation du glucose, métabolite
- Activité 2.1 QCM: Audit interne et auditeur
- Activité 2.odt: La biodiversité dans le monde
- Explication de texte autour d'un extrait de l'ouvrage Le poète et l'activité de la fantaisie, de Sigmund Freud