16/03/2012 Dérivés Carbonylés 1 Propriétés Chimiques C + C O C - Présence de doublets sur l'oxygène Basicité (pKa -6 à
Publié le 02/10/2014
Extrait du document
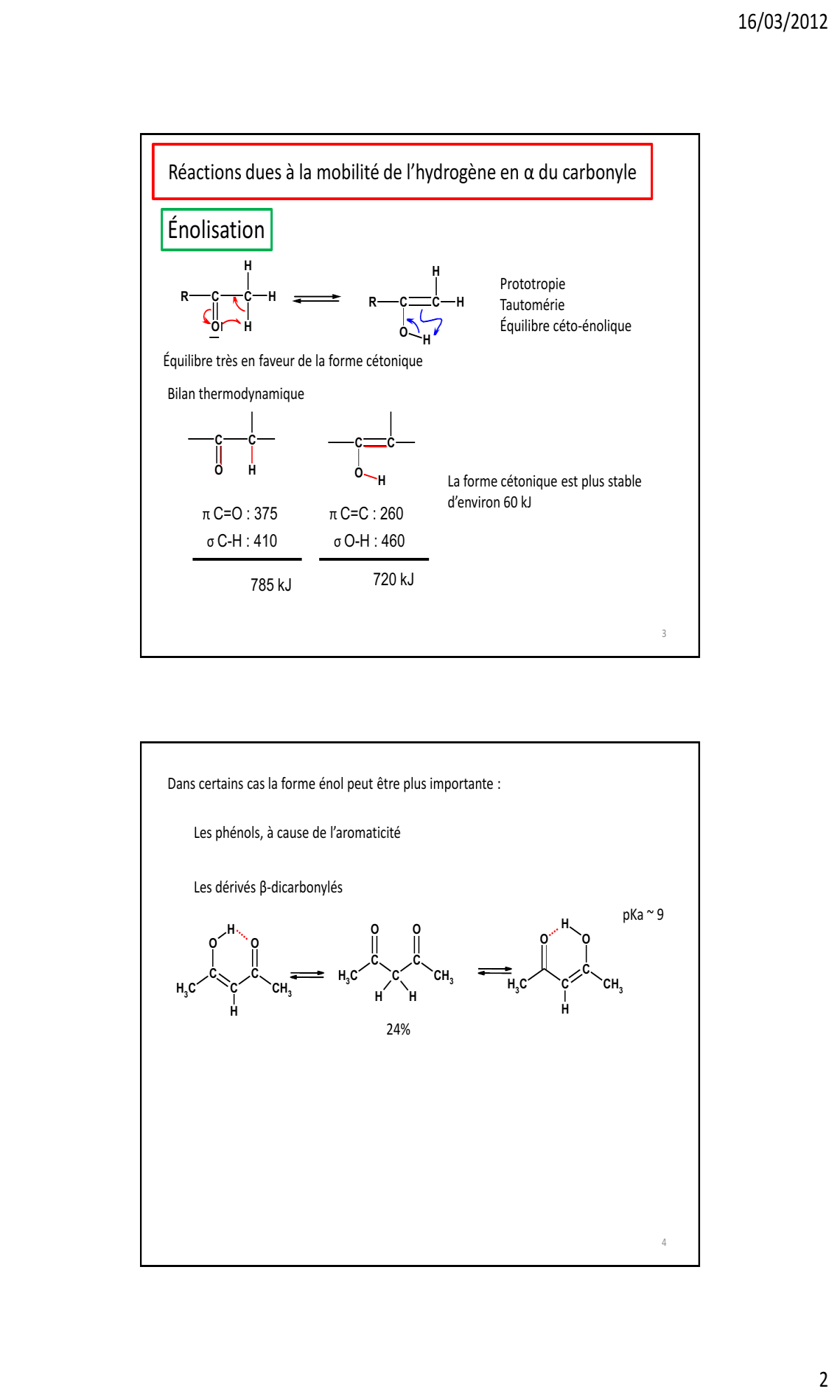
« 16/03/2012 2 Réactions dues à la mobilité de l’hydrogène en α du carbonyle Énolisation Prototropie Tautomérie Équilibre céto -énolique Équilibre très en faveur de la forme cétonique Bilan thermodynamique π C=O : 375 σ C-H : 410 785 kJ π C=C : 260 σ O-H : 460 720 kJ La forme cétonique est plus stable d’environ 60 kJ 3 Dans certains cas la forme énol peut être plus importante : Les phénols, à cause de l’aromaticité Les dérivés β-dicarbonylés 24% pKa ~ 9 4 R C O C H H H R C O C H H H C O C H C O C H C H 3 C C C C H 3 O O H H C H 3 C C C C H 3 O O H H C H 3 C C C H 3 O O H H. »
↓↓↓ APERÇU DU DOCUMENT ↓↓↓
Liens utiles
- 07/11/2011 Les dérivés Carbonylés H,C C O H,C 1 Nomenclature CO Groupement carbonyle : CO lié uniquement à C ou H O Les aldéhydes C H Au moins un des deux substituants est un atome d'Hydrogène Groupement principal : suffixe al, ou carbaldéhyde pour des molécules complexes H CHO H3C CHO Méthanal (ou aldéhyde formique ou formaldéhyde) (la solution aqueuse à 40% = formol) Éthanal ( ou aldéhyde acétique ou acétaldéhyde) CHO Cyclohexane carbaldéhyde Groupement secondaire
- 16/03/2012 Les Phénols Le phénol 1 Propriétés Chimiques Acidité, coupure de la liaison O-H 2 doublets non liants basicité nucléophilie Liaison C-O polaire : coupure ?
- 22/03/2012 Les amines 1 Propriétés Chimiques Pour les trois classes d'amines N La présence d'un doublet
- Les composés halogénés 1- Généralités Nomenclature Propriétés physico-chimiques Réactivité 2- Réactions 2.
- 07/11/2011 Acides aminés et dérivés Définition : Dérivés bifonctionnels - fonction acide carboxylique - fonction amine Seulement 20 (21) amino acides naturels entrent dans la composition des protéines, traduits du code génétique supporté par les acides nucléiques Dans certains cas, des acides aminés pourront - après formation de la protéine - subir des modifications dites post translationnelles La composition en AA des protéines matures est donc un peu plus complexe 1 Structure