Les catalyseurs
Publié le 17/01/2022
Extrait du document
Les catalyseurs sont des molécules chimiques qui peuvent prendre trois formes différentes : solide, liquide ou gazeux. Dans les processus naturels de la vie ou dans l'industrie chimique, ils ont un même rôle : accélérer la vitesse des réactions. On les utilise par exemple pour les multiples transformations du pétrole.
«
SCIENCES LES CATALYSEURS
Des catalyseurs
à tous les niveaux
La plupart des réactions qui se produisent
dans le milieu vivant, animal ou végétal ,
et qui assurent les fonctions vitales ainsi que
la croissance, sont catalysées par des
enzymes .
Ces composés
sont synthétisés
par
les cellules elles-mêmes .
Par exemple,
le glucose ,
un sucre de notre alimentation ,
est transformé en énergie , indispensable
à notre organisme .
Sans catalyseur, cette
transformation ne se ferait qu'à une
température très élevée que nous ne
pourrions pas supporter.
L'homme utilise
également le
pouvoir des catalyseurs
biologiques
dans sa vie quotidienne :
les enzymes produites par diverses levures,
qui sont des champignons unicellulaires ,
servent à transformer le raisin en vin, à faire
lever le pain ou à affiner les fromages .
La nature : économe en énergie
L'ammoniac est un produit nécessaire à une
bonne
fertilisation des sols , il est le produit
de base de nombreux
engrais .
Dans la
nature, dans
des conditions
de
température et
gaz
de pression ordinaires, du moteur
il est fabriqué par des
bactéries
et leurs enzymes qui forment
des nodosités (des nceuds) sur les racines
de trèfle .
Si l'Homme a bien compris ce
que fait
la nature, il lui faut utiliser beaucoup
d'énergie
pour obtenir le même résultat.
Ainsi , l'industrie chimique doit travailler à
une
température de 350 °c et une pression
200 fois supérieure à la pression
atmosphérique
normale , malgré l'utilisation
d'un catalyseur à base de fer.
Un catalyseur
pour une réaction
Pour les chimistes, il n'existe pas de règles
simples
et sûres pour prévoir quel
catalyseur
convient à une réaction
particulière .
Ils sont obligés de « tâtonner »
EN SAVOIR PLUS
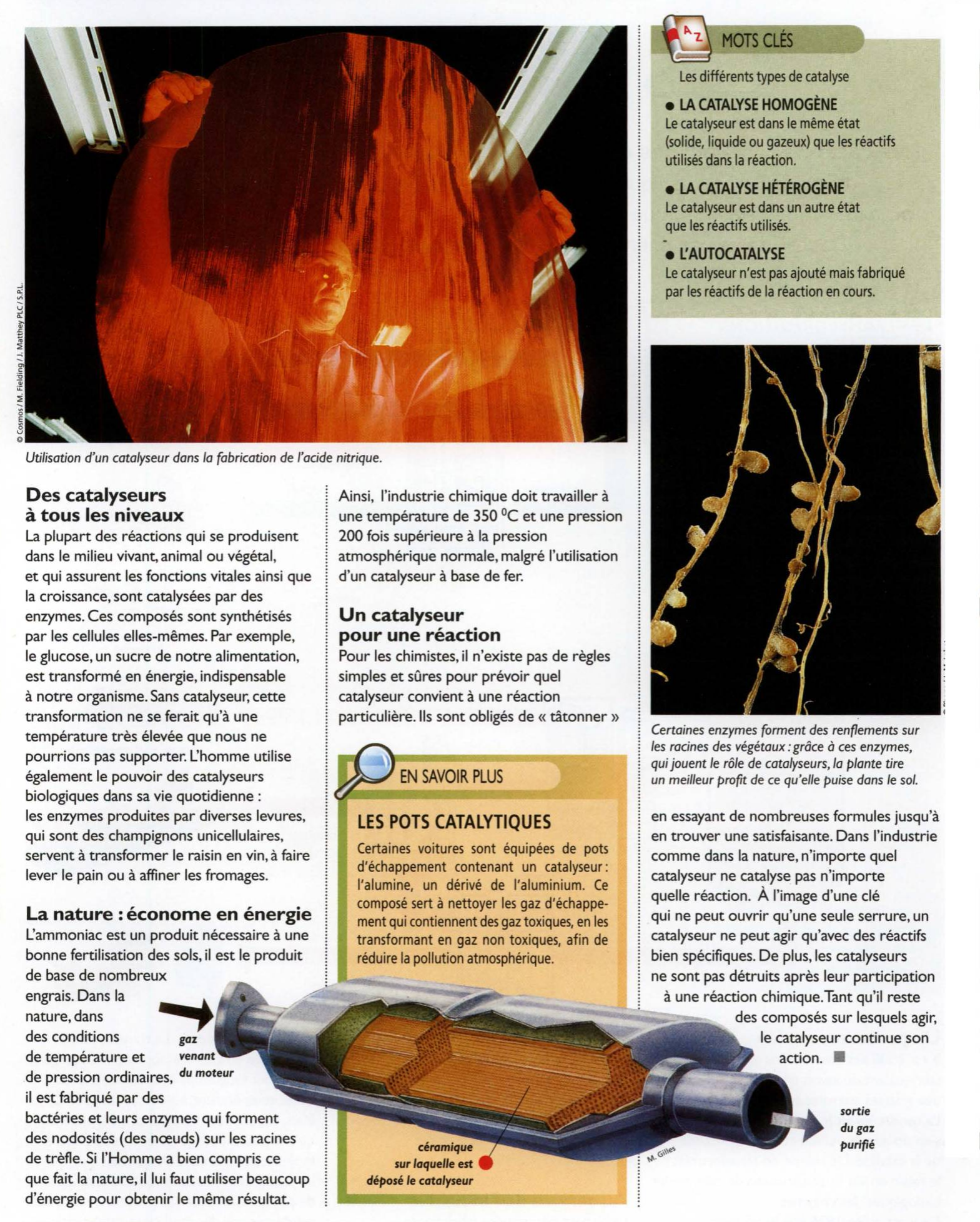
LES POTS CATALYTIQUES
Certaines voitures sont équipées de pots
d'échappement contenant un catalyseur :
l'alumine,
un dérivé de l'aluminium.
Ce
composé sert à nettoyer les gaz d'échappe
ment
qui contiennent des gaz toxiques, en les
transformant en gaz non toxiques, afin de
réduire la pollution atmosphérique.
VOIR AUSSI : • Histoire de la chimie/ Le laboratoire de chimie/ Atomes et molécules
• La transformation de l'énergie • Vie et énergie
240 •
• LA CATALYSE HOMOGÈNE
Le catalyseur est dans le même état
(solide, liquide ou gazeux) que les réactifs
utilisés dans la réaction .
• LA CATALYSE HÉTÉROGÈNE
Le catalyseur est dans un autre état
que les réactifs utilisés .
• L'AUTOCATALYSE
Le catalyseur n'est pas ajouté mais fabriqué
par les réactifs de la réaction en cours.
Certaines enzymes forment des renflements sur /es racines des végétaux : grâce à ces enzymes , qui jouent le rôle de catalyseurs , la plante tire un meilleur profit de ce qu'elle puise dans le sol.
en essayant de nombreuses formules jusqu'à
en
trouver une satisfaisante .
Dans l'industrie
comme dans la nature, n' importe quel
catalyseur
ne catalyse pas n 'importe
quelle réaction .
À l'image d 'une clé
qui ne peut ouvrir qu'une seule serrure, un
catalyseur ne peut agir qu'avec des réactifs
bien spécifiques.
De plus, les catalyseurs
ne sont pas détruits après leur participation
à une réaction chimique .Tant
qu'il reste
des composés
sur lesquels agir,
le catalyseur continue son
action .
•
sortie du gaz purifié.
»
↓↓↓ APERÇU DU DOCUMENT ↓↓↓